前立腺がん診断の精度を飛躍的に高める国産の新規診断法「S2,3PSA%検査」の共同開発と実用化について
2022.09.26
研究
弘前大学大学院医学研究科 泌尿器科学講座の大山 力 教授と糖鎖工学講座の米山 徹 助教らの研究チームは、腫瘍マーカー「前立腺特異抗原(PSA)」タンパク質上の糖鎖構造の詳細な構造解析から、前立腺細胞のがん化によってPSAタンパク質上の糖鎖構造の末端シアル酸の結合様式の含有量が変化することを発見し、非がん患者由来PSAをS2,6PSA、がん患者由来PSAをS2,3PSAと命名し、「S2,3PSA」を腫瘍マーカーとして臨床応用する研究を進めており、2022(令和4)年9月26日に記者発表を行いました。
プレスリリース内容
本件のポイント
- 研究チームは、富士フイルム和光純薬株式会社の協力を受け、S2,3PSA%検査として、マイクロキャピラリー電気泳動技術を利用し、血液中のS2,3PSAとS2,6PSAの濃度を定量することで前立腺癌の診断補助に利用できる新規体外診断用医薬品「ミュータスワコー S2,3PSA・i50」を共同開発しました。臨床性能試験の結果から、従来のPSA検査で陽性(PSA検査値4 ng/mL 以上)となっても実際は前立腺がんではない方(偽陽性)と真に前立腺がんである患者さんを従来のPSA検査よりも、より高精度に識別可能であることを明らかにしました。グレーゾーンと呼ばれるPSA 低値陽性群(PSA検査値4〜10 ng/mL)で偽陽性率が高く、世界的な社会問題となっているPSA検査に対して、「S2,3PSA%検査」を二次血液検査として実施すれば、がんではない人が不要な針生検など侵襲性の高い精密検査を受ける不利益を回避できると期待されます。
- 「ミュータスワコー S2,3PSA・i50」は、富士フイルム和光純薬株式会社にて、2022年 8 月 22 日に厚生労働省から新規体外診断用医薬品として製造販売承認を受け、臨床現場で使用可能となりました。今後、S2,3PSA%検査の保険収載に向けて、さらに研究を進め、国産で初めての前立腺がん腫瘍マーカー検査として、広く普及活動を展開していく予定です。
研究の背景と目的
前立腺がんは特に欧米などで発症頻度の高いがんですが、近年日本でも前立腺がんの罹患数、死亡数が急速に増加しています。2019年 全国がん登録 罹患数・率報告(厚生労働省健康局がん・疾病対策課)によると年間94,748人が罹患し、もっとも多い男性がんとなっています。がん統計予測(国立がん研究センター・がん情報サービスの公開しているデータ)によると2022年の前立腺がん死亡数は、年間13,300人と予測され、男性がんの6番目で、多少の変動はあるものの増加傾向にあります。米国では、死亡数の高さから社会問題になっている前立腺がんですが、1990年代の罹患数、死亡数の日米間格差は、23倍と7倍でした。しかし2018年のデータの比較では、それらがともに2倍まで差が縮まっています。今後も高齢化社会の進行に伴いさらに増加するとも予測されています。日米の人口比を考慮すると、本邦における前立腺がんに対する適切なマネージメントは喫緊の重要な課題です。
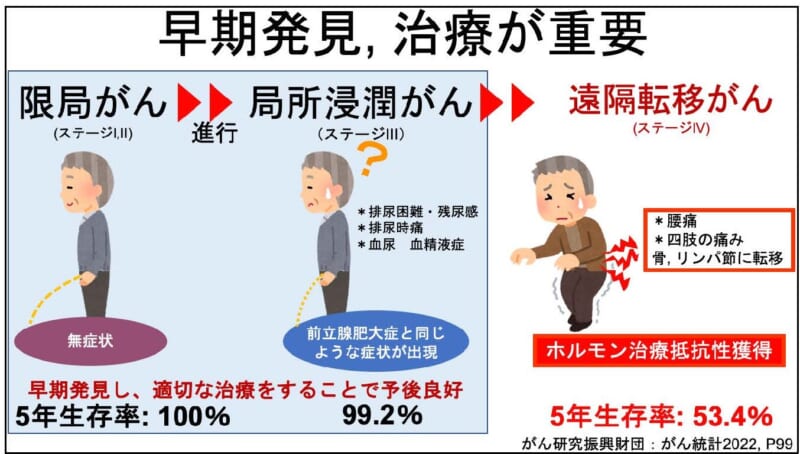
前立腺がんは多くの場合、比較的ゆっくり進行し、手術や内分泌(ホルモン)療法など確立された治療法も存在するため、早期に発見し、適切な治療をすれば5年生存率は、前立腺に限局するがん(ステージ I,II)で 100%、局所浸潤がん(ステージ III)で99.2%と良好な予後が期待できるがんです。しかし発見が遅れ、リンパ節や骨に転移したがん(ステージ IV)となると5年生存率は、53.4%と著しく低下してしまうことから、早期発見が非常に重要ながんであるといえます(図1)。
欧米で実施された無作為化比較対照試験の結果から国家レベルで前立腺がんの死亡率を低下させるには、早期発見・適切治療が有効であることがすでに証明されていますが、より有効かつ効率の良い前立腺がん診断システムの確立には、がんの悪性度が高く即時治療が必要な「臨床的に重要な前立腺がん」の正確な診断が欠かせません。
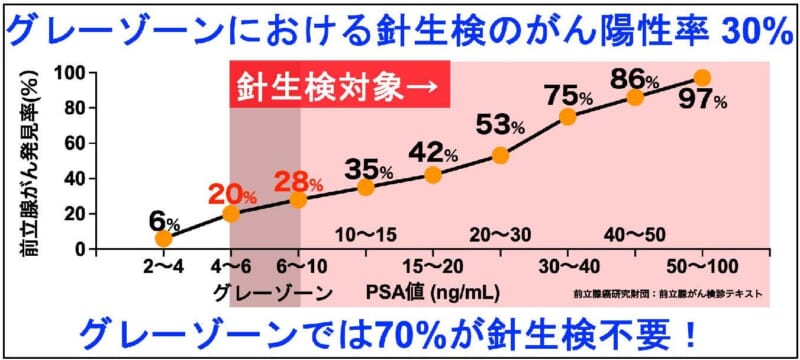
1990年代に米国で開発された PSA検査の導入によって非常に早期の前立腺がんまで検出が可能になった一方で、逆にがんではない方も多く陽性を示してしまうこと(偽陽性)が問題となっています。PSAは前立腺がんだけではなく、前立腺肥大症、前立腺炎のような他の前立腺疾患においても過剰に産生されることが知られています。通常、PSA 検査値が4ng/mL 以上となると精密検査の受診対象となりますが、特にPSA検査値4~10 ng/mL の「グレーゾーン」と呼ばれる領域では 70%程度が実際はがんではなかったという疫学データが報告されています(図2)。
PSA 検査が陽性となり、精密検査の受診を勧められた場合、経直腸前立腺触診や入院を必要とする前立腺針生検といった肉体的、精神的に苦痛を伴う検査を受診することとなり、がんが見つからなかった場合は受診者側にも医療者側また医療経済的にも不要な負担がかかります。
このような背景から、治療が必要な前立腺がん患者さんをより正確に診断できる簡便な検査法が必要とされていました。そこで、研究チームは前立腺がん診断の精度(がん特異性)を飛躍的に高めることが可能な国産の新規診断法の開発を試みました。
研究の成果
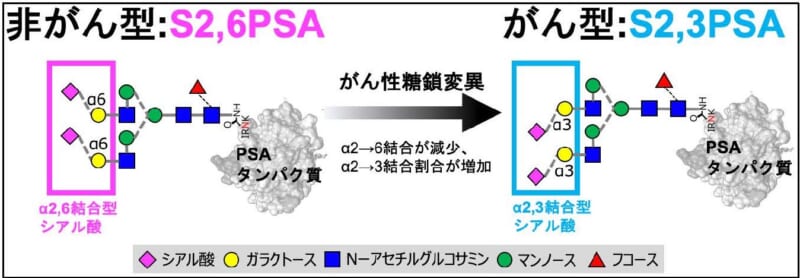
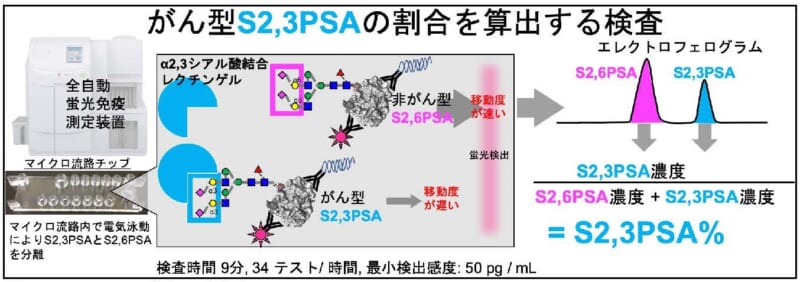
大山 力 教授(弘前大学大学院医学研究科 泌尿器科学講座)、米山 徹 助教 (同大学院医学研究科 糖鎖工学講座)らの研究チームは、PSAタンパク質上の糖鎖構造の詳細な構造解析から、前立腺細胞のがん化によってPSAタンパク質上の糖鎖構造の末端シアル酸の結合様式の存在比(非がん型:S2,6PSAとがん型:S2,3PSAの割合)が変化することを見出しました(図3)。
健常な人や前立腺肥大症などの良性疾患の患者の血清由来PSAの糖鎖末端はシアル酸α 2,6ガラクトース構造が多く、前立腺がん患者の血清由来PSAの糖鎖末端はシアル酸α2,3ガラクトース構造が増加しました。そこで、非がん型PSAをS2,6PSA、がん型PSAをS 2,3PSAと命名しました。
この知見をもとに富士フイルム和光純薬株式会社との共同研究により、S2,3PSA%検査としてマイクロキャピラリー電気泳動技術を基盤とした全自動蛍光免疫測定装置「ミュータスワコーi50」を用いた血液中のがん型S2,3PSAの割合(S2,3PSA%)を定量する体外診断用医薬品「ミュータスワコー S2,3PSA・i50」を開発しました(図4)。
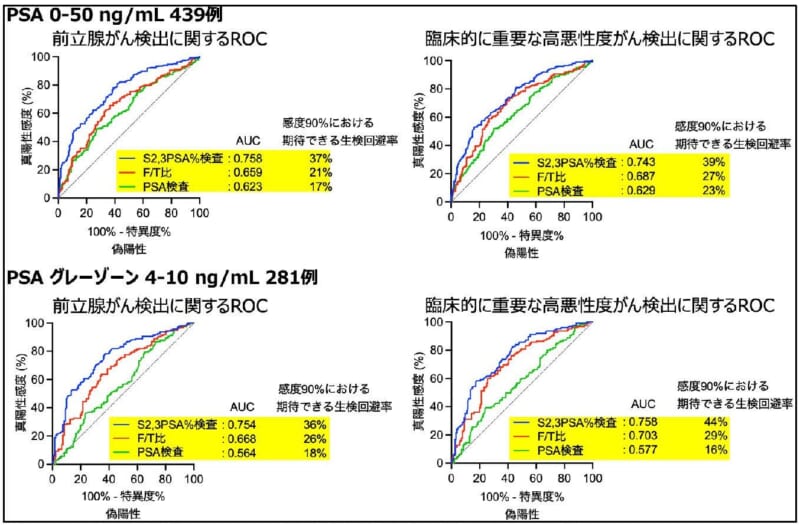
同体外診断用医薬品の多施設共同臨床性能試験のために、国内7施設において前立腺がん疑いとして受診した合計439名の患者(うち281名がPSA検査値グレーゾーン)から採取した血清検体に対してS2,3PSA%検査を実施し、現在、保険適応されているPSA検査およびF/T比検査の前立腺がん診断精度を検査特異度(期待できる針生検回避率)および受信者動作特性曲線(ROC)解析によるROC曲線下面積(AUC)値で比較しました。その結果、(図5)に示す通り、前立腺がんの検出に関するS2,3PSA%検査のAUC値は、PSA検査値に関係なく、本邦保険診療で使用可能なPSA検査およびF/T比のAUC値より統計的に有意に高い結果が得られ、「90%の感度を維持しながら、36〜37%の針生検回避を期待できる」との有益な結果を示しました。
また、「悪性度が高い臨床的に重要な前立腺がん」の検出に関するS2,3PSA%検査のAU C値も上記と同様に本邦保険診療で使用可能なPSA検査およびF/T比のAUC値より統計的に有意に高い結果が得られ、「90%の感度を維持しながら、39〜44%の針生検回避が期待できる」との有益な結果を示しました。悪性度が高い臨床的に重要な前立腺がんの検出特異度が優れていることから、将来的にS2,3PSA%検査は前立腺がんの悪性度診断の補助的な指針、もしくは予後マーカーとなりうる可能性も期待できます。
まとめと今後の展開
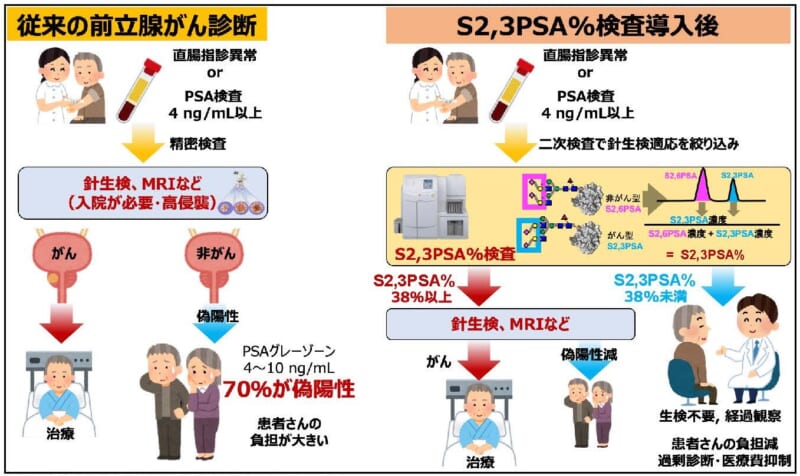
前立腺がん診断の精度を高めることができる新たな糖鎖標的を利用した前立腺腫瘍マーカーS2,3PSA%検査を開発しました。S2,3PSA%検査は採血のみで結果が出ることから、低侵襲的で簡便ながら針生検を含む精密検査の受診を要する患者の絞り込みが可能で、患者の不利益を回避しつつ、医療経済的にも優れた腫瘍マーカーとして期待されております(図6)。今後は、S2,3PSA%検査の保険収載を目指し、臨床での使用を通じて、あるいは研究の一環として、多くの先生方がS2,3PSA%検査を用いた様々なアイデアでの研究を実施していただき、S2,3PSA%検査のパフォーマンスを臨床現場で使い切ることができるように、活躍の場が増えることを期待しています。
本研究成果は前立腺の解剖学、生理学、病理学を専門とする医学雑誌である「The Prostate」オンライン版(2021年9月21日)に掲載されました。
腫瘍マーカー検査
腫瘍マーカーとは、がんの種類によって特徴的に作られるタンパク質などの物質。がん細胞やがん細胞に反応した細胞によって作られ、血中や尿中に分泌される。このタンパク質の分泌量を調べる検査を腫瘍マーカー検査と言い、がんの診断の補助や、診断後の経過や治療の効果をみることを目的に行う。がんの有無やがんがある場所は、腫瘍マーカーの値だけでは確定できないため、画像検査など、その他の検査の結果も合わせて、医師が総合的に判断する。
糖鎖
DNA、RNA(核酸)、タンパク質に続く第3の生命鎖と呼ばれる分子。単糖(シアル酸、ガラクトース、グルコサミン、マンノースなど)が鎖状につながったもので細胞を構成するタンパク質、脂質などに付加され、細胞の機能を調節する役割を持つ。細胞表面にヒゲのように付加されている。
前立腺特異抗原 prostate specific antigen (PSA)
前立腺上皮細胞から前立腺腔内に分泌されるタンパク質。前立腺がんとなり前立腺組織が破壊されると血液中に漏れ出てくる。前立腺がんの腫瘍マーカーとして1990年代から利用されている。血液検査によりPSA検査値が4ng/mL以上を超えると針生検などの精密検査対象となる。PSA検査値4〜10 ng/mLの範囲は、グレーゾーンと呼ばれ、偽陽性が多く問題となっている。PSAは糖鎖が付加されている糖タンパク質である。
臨床的に重要な前立腺がん
組織の悪性度が高く、手術や放射線治療、ホルモン治療など、積極的な治療介入が必要な前立腺がん。
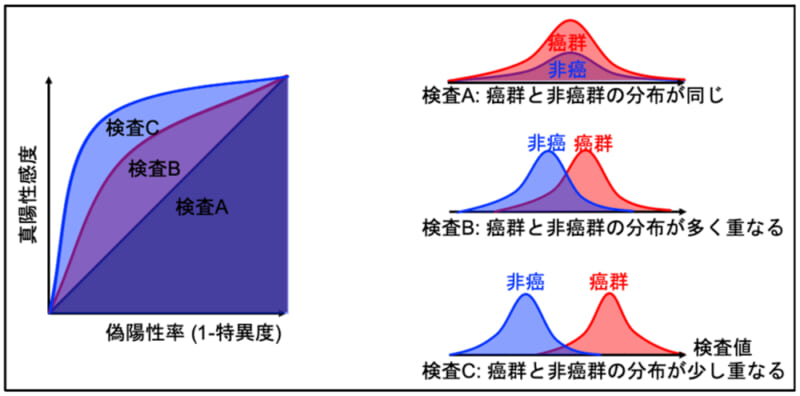
受信者動作特性曲線(ROC)解析とAUC
検査の感度と特異度の関係を視覚的に表す解析方法。ROC理論は第2次世界大戦中に、レーダーのノイズから敵機を正しく検出するために考え出された理論。縦軸を検査の「真陽性感度」とし、横軸を検査の「偽陽性率(1一特異度)」としたグラフ。曲線下面積 Area under the curve (AUC) が1.0に近づけば近づくほど検査精度が高いと評価できる。
原著論文情報
原著論文タイトル
Characteristics of α2,3-sialyl N-glycosylated PSA as a biomarker for clinically significant prostate cancer in men with elevated PSA level
掲載紙名
The Prostate
著者
米山 徹(1)、山本勇人(2)、飛澤悠葵(2)、米山美穂子(3)、畠山真吾(2,4)、成田拓磨(2)、小玉寛健(2)、百田匡毅(2)、伊藤弘之(5)、成田伸太郎(6)、対馬史泰(7)、三塚浩二(8)、米山高弘(2,9)、橋本安弘(2)、Wilhelmina Duivenvoorden(10)、Jehonathan H Pinthus(10)、掛田伸吾(7)、伊藤明宏(8)、土谷順彦(11)、羽渕友則(6)、大山 力(2,4,9)※責任著者
1)弘前大学大学院医学研究科 附属高度先進医学研究センター 糖鎖工学講座
2)弘前大学大学院医学研究科 泌尿器科学講座
3)鷹揚郷腎研究所 癌免疫細胞生物学研究部
4)弘前大学 大学院医学研究科 先進血液浄化療法学講座
5)青森労災病院 泌尿器科
6)秋田大学大学院医学系研究科 腎泌尿器科学講座
7)弘前大学大学院医学研究科 放射線診断学講座
8)東北大学大学院医学系研究科 外科病態学講座 泌尿器科学分野
9)弘前大学大学院医学研究科 先進移植再生医学講座
10)Department of Surgery, McMaster University, Hamilton, Ontario, Canada.
11)山形大学大学院医学研究科 腎泌尿器外科学講座
文部科学省科学研究費補助金 基盤研究(A) 15H02563、挑戦的萌芽研究15H15579
■ プレスリリース資料は こちら(3.2MB)





 背景色
背景色 文字サイズ
文字サイズ Language
Language アクセス
アクセス お問い合わせ
お問い合わせ